Giáo án môn Hóa học lớp 10 - Tiết 60: Kiểm tra 1 tiết
I/ Mục tiêu bài học
1 -Kiến thức: Củng cố hệ thống toàn bộ nội dung của toàn chương ôxi - lưu huỳnh.
2 - Kỹ năng: Làm bài độc lập sáng tạo
3 - Thái độ: Nghiêm túc tự giác
II/ Chuẩn bị:
- Giáo viên: Đề, đáp án
- HS: Giấy bút
III/ Tiến trình lên lớp:
1 - Kiểm tra bài cũ: Không
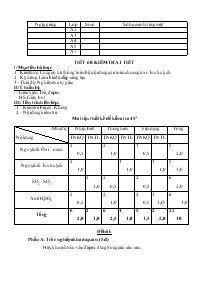
2 - Nội dung kiểm tra:
Bạn đang xem tài liệu "Giáo án môn Hóa học lớp 10 - Tiết 60: Kiểm tra 1 tiết", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
Ngày giảng Lớp Sĩ số Số học sinh vắng mặt A2 A3 A4 A5 A7 TIẾT 60: KIỂM TRA 1 TIẾT I/ Mục tiêu bài học 1 -Kiến thức: Củng cố hệ thống toàn bộ nội dung của toàn chương ôxi - lưu huỳnh. 2 - Kỹ năng: Làm bài độc lập sáng tạo 3 - Thái độ: Nghiêm túc tự giác II/ Chuẩn bị: - Giáo viên: Đề, đáp án - HS: Giấy bút III/ Tiến trình lên lớp: 1 - Kiểm tra bài cũ: Không 2 - Nội dung kiểm tra: Ma trận thiết kế đề kiểm tra 45' Mức độ Nội dung Nhận biết Thông hiểu Vận dụng Tổng TNKQ TNTL TNKQ TNTL TNKQ TNTL Nguyên tố Ô xi - ozon 2 0,5 2 1,0 1 0,5 5 2,0 Nguyên tố lưu huỳnh 2 1,0 1 1,0 1 1,0 5 3,0 SO2 - SO3 2 1,0 2 0,5 2 0,5 6 2,0 Axit H2SO4 2 0,5 2 1,0 2 0,5 1 1,O 6 3,0 Tổng 6 2,0 2 1,0 6 2,5 1 1,0 5 1,5 2 2,0 22 10 Đề bài: Phần A: Trắc nghiệm khách quan: (5 đ) - Hãy khoanh tròn vào đáp án đúng trong các câu sau: Câu 1: (0,5 đ) Để chuyển hoá hoàn toàn 4,8 g lưu huỳnh thành lưu huỳnh đi ôxít (SO2) thì thể tích không khí (ĐKTC) cần dùng là. A, 15,8 lít B, 16,8 lít C, 17,8 lít D, 18,8 lít Câu 2: (0,25 đ) Ôxi không tác dụng với chất nào ở t0 thường? A, Au B, Al C, Fe D, Zn Câu 3:(0,5) Trộn 11,7 g kali với một lượng dư kim loại ở nhóm VI A đun nóng hỗn hợp trong bình kín không có ôxi, thu được 16,5 g muối tên kim loại đó là: A, Lưu huỳnh B, ôxi C, Selen D, Telu Câu 4:(0,25) Ở dạng đơn chất và hợp chất lưu huỳnh có các số ôxi hoá nào? A, - 2; + 4; + 5; + 6 C, + 1; 0;+ 4; +6 B, - 3; + 2; + 4; + 6 D, 0; - 2; + 4 + 6 Câu 5:(0,5) Một hợp chất sunphua của kim loại R hoá trị III trong đó lưu hùnh chiếm 64% theo khối lượng. Tên kim loại R là A, Al B, Au C, Fe D, Ag Câu 6:(0,25) Khí O 2 khi điều chế có lẫn 1 lượng hơi nước. Để loại nước ra khỏi O2 thì sử dụng chất nào trong các chất sau: A, Al2O3 B, H2SO4 C, CuSO4 D, KOH Câu 7:(O,25) Chất nào sau đây vừa có tính ôxi hoá vừa có tính khử? A, H2S B, H2SO4 C, SO2 D, CaCO3 Câu 8:(0,5) Cho một ptg SO3 vào một cốc nước, sau đó thêm nước vào để được 0,5 lít dung dịch A. Nồng độ của dung dịch A là: A, 2M B, 3M C, 4M D, 5M Câu 9:(0,25) Cặp chât nào sau đây có thể tồn tại trong một hỗn hợp ở nhiệt độ thường? A, Cl2 và H2S B, SO2 và O3 C, SO2 và O2 D, Na2CO3 và H2SO4 Câu 10:(0,5) Cho 4 dung dịch đựng trong 4 lọ mất nhãn sau: HCl; CaSO4; KCl; Ba(OH)2 chỉ dùng một thuốc thử trong các thuốc thử sau để nhận biết. A, H2SO4 B, AgNO3 C, BaCl2 D, Quỳ tím Câu 11:(0,5) Dung dịch H2SO4 35% (d = 1,4 g/ml). Nồng độ mol của dung dịch này là: A, 5 mol/l B, 6 mol/l C, 7 mol/l D, 8 mol/l Câu 12:(0,25) Khí sunphuarơ (SO2) được điều chế từ: A, Cu + H2SO4 C, Pb + O2 B, NaSO3 + HCl D, Tất cả đều đúng B, Tự luận (5 đ) Câu 1: (2 đ) Thực hiện chuỗi phản ứng sau: SO2 (1) H2SO4 (2) Al2(SO4)3 (3) AlCl3 (4) Al(NO3)3 Câu 2: (3 đ) Ôxi hoá hoàn toàn 4,8 g lưu huỳnh bằng ozon, thu được chất hoá lỏng A. Hoà tan A vào 1 lít nước. Tính nồng độ % của dung dịch thu được. ĐÁP ÁN- THANG ĐIỂM Phần A: Trắc nghiệm khách quan (5 đ) 1 - B; 0,5 4 - D; 0,5 7 - C; - 0,25 10 - D; 0,5 2 - A; 0,25 5 - A; 0,5 8 - A; 0,5 11 - A; 0,5 3 - A; 0,5 6 - B; - 0,25 9 - C; - 0,25 12 - D; 0,5 Phần B: Tự luận: (5 đ) Câu 1 (2 đ) Thực hiện chuỗi phản ứng sau: (1) SO2 + Br2 + 2H2O H2SO4 + 2HBr (0,5 đ) (2) 3H2SO4 + 2Al(OH)3 Al2(SO4)3 + 6H2O (0,5 đ) (3) Al2(SO4)3 + 3BaCl2 3BaSO4 + 2 AlCl3 (0,5 đ) (4) AlCl3 + 3AgNO3 Al(NO3)3 + 3 AgCl (0,5 đ) Câu 2: (3 đ) (0,5 đ) phản ứng S + O3 SO3 (1) (0,5 đ) (mol) 0,15 0,15 SO3 + H2O H2SO4 (2) (0,25 đ) Từ (1) và (2) (0,75 đ) Khối lượng dung dịch thu được: (0,5 đ) Vậy C% H2SO4 = (0,5 đ) 3.Củng cố:-Thu bài ,nhận xét giờ kiểm tra. 4.Dặn dò:-Xem lại bài,đọc trước bài Tốc độ PU hoá học. TRƯ ỜNG THPT XUÂN HUY Họ và tên:................................. Điểm Lớp:................................ KIỂM TRA MỘT TIẾT Lời phê của Cô giáo Môn: Hóa học Đề bài: Phần A: Trắc nghiệm khách quan: (5 đ) - Hãy khoanh tròn vào đáp án đúng trong các câu sau: Câu 1: (0,5 đ) Để chuyển hoá hoàn toàn 4,8 g lưu huỳnh thành lưu huỳnh đi ôxít (SO2) thì thể tích không khí (ĐKTC) cần dùng là. A, 15,8 lít B, 16,8 lít C, 17,8 lít D, 18,8 lít Câu 2: (0,25 đ) Ôxi không tác dụng với chất nào ở t0 thường? A, Au B, Al C, Fe D, Zn Câu 3:(0,5) Trộn 11,7 g kali với một lượng dư kim loại ở nhóm VI A đun nóng hỗn hợp trong bình kín không có ôxi, thu được 16,5 g muối tên kim loại đó là: A, Lưu huỳnh B, ôxi C, Selen D, Telu Câu 4:(0,25) Ở dạng đơn chất và hợp chất lưu huỳnh có các số ôxi hoá nào? A, - 2; + 4; + 5; + 6 C, + 1; 0;+ 4; +6 B, - 3; + 2; + 4; + 6 D, 0; - 2; + 4 + 6 Câu 5:(0,5) Một hợp chất sunphua của kim loại R hoá trị III trong đó lưu hùnh chiếm 64% theo khối lượng. Tên kim loại R là A, Al B, Au C, Fe D, Ag Câu 6:(0,25) Khí O 2 khi điều chế có lẫn 1 lượng hơi nước. Để loại nước ra khỏi O2 thì sử dụng chất nào trong các chất sau: A, Al2O3 B, H2SO4 C, CuSO4 D, KOH Câu 7:(O,25) Chất nào sau đây vừa có tính ôxi hoá vừa có tính khử? A, H2S B, H2SO4 C, SO2 D, CaCO3 Câu 8:(0,5) Cho một ptg SO3 vào một cốc nước, sau đó thêm nước vào để được 0,5 lít dung dịch A. Nồng độ của dung dịch A là: A, 2M B, 3M C, 4M D, 5M Câu 9:(0,25) Cặp chât nào sau đây có thể tồn tại trong một hỗn hợp ở nhiệt độ thường? A, Cl2 và H2S B, SO2 và O3 C, SO2 và O2 D, Na2CO3 và H2SO4 Câu 10:(0,5) Cho 4 dung dịch đựng trong 4 lọ mất nhãn sau: HCl; CaSO4; KCl; Ba(OH)2 chỉ dùng một thuốc thử trong các thuốc thử sau để nhận biết. A, H2SO4 B, AgNO3 C, BaCl2 D, Quỳ tím Câu 11:(0,5) Dung dịch H2SO4 35% (d = 1,4 g/ml). Nồng độ mol của dung dịch này là: A, 5 mol/l B, 6 mol/l C, 7 mol/l D, 8 mol/l Câu 12:(0,25) Khí sunphuarơ (SO2) được điều chế từ: A, Cu + H2SO4 C, Pb + O2 B, NaSO3 + HCl D, Tất cả đều đúng B, Tự luận (5 đ) Câu 1: (2 đ) Thực hiện chuỗi phản ứng sau: SO2 (1) H2SO4 (2) Al2(SO4)3 (3) AlCl3 (4) Al(NO3)3 Câu 2: (3 đ) Ôxi hoá hoàn toàn 4,8 g lưu huỳnh bằng ozon, thu được chất hoá lỏng A. Hoà tan A vào 1 lít nước. Tính nồng độ % của dung dịch thu được. BÀI LÀM:
Tài liệu đính kèm:
 kiem tra.doc
kiem tra.doc





